北京市药品监督管理局关于批准注册57个第二类医疗器械产品的公告 (2025年5月) 医护人员防护用品
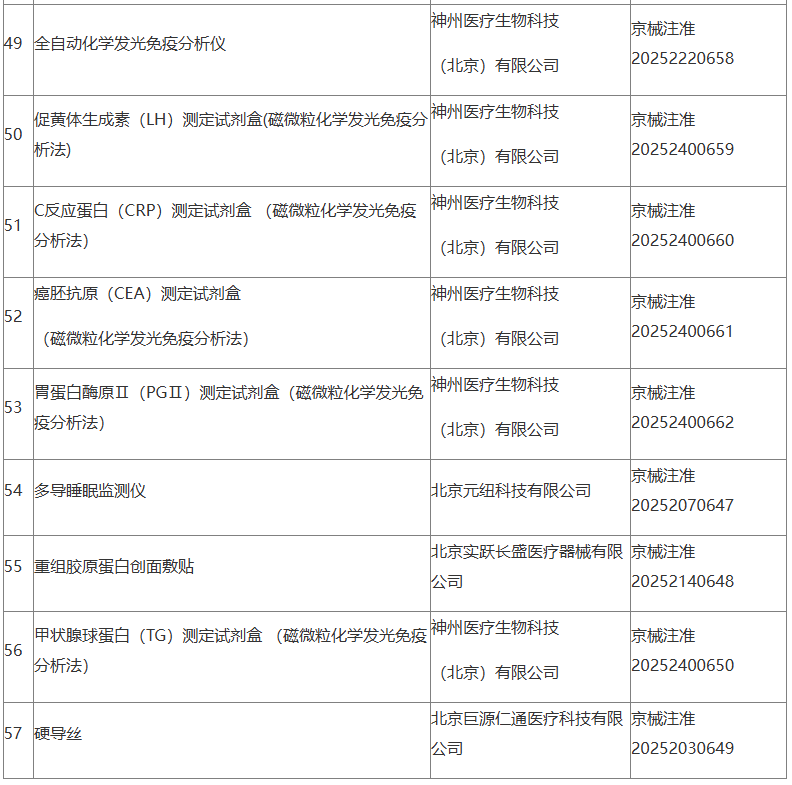
根据《医疗器械监督管理条例》及相关法规要求,经北京市药品监督管理局审查,现批准注册57个第二类医疗器械产品,具体信息公告如下。
一、 总体情况
本次公告(2025年5月)批准注册的第二类医疗器械产品共计57个,涵盖多个临床急需领域,其中医护人员防护用品是本次获批的重点品类之一。这体现了北京市持续加强公共卫生应急物资保障能力、提升医疗服务质量安全水平的坚定决心,也是落实国家关于完善公共卫生应急管理体系、保障医护人员职业安全健康相关部署的重要举措。
二、 获批产品特点
本次获批的医护人员防护用品主要包括:
- 医用防护口罩:多款产品在过滤效率、密合性、呼吸阻力等关键性能指标上达到或优于国家标准,为高风险环境下的医护人员提供有效呼吸防护。
- 医用防护服/隔离衣:采用新型复合材料,在保证液体阻隔性能的提升了透气性和穿着舒适度,有助于医护人员长时间穿戴执行任务。
- 医用外科口罩:注重佩戴舒适性与防护效果的平衡,满足日常诊疗及一般手术环境下的防护需求。
- 医用隔离眼罩/面罩:增强了防雾、抗冲击性能,提供全面的面部及眼部保护。
- 医用隔离鞋套/帽:完善了全身防护的闭环,减少交叉感染风险。
这些产品均经过严格的注册检验、临床评价(如适用)和技术审评,符合医疗器械安全、有效的基本要求,其生产企业的质量管理体系也通过了现场核查。
三、 重要意义
- 保障医护安全:高质量的防护用品是保障一线医务人员生命健康与职业安全的第一道防线,本次批量获批丰富了市场供应选择,提升了整体防护水平。
- 优化产业布局:鼓励和引导本地及国内企业研发生产高性能防护产品,促进了北京市乃至全国医疗器械产业在防护领域的创新发展与供应链韧性。
- 强化应急储备:为应对可能发生的公共卫生事件,建立和完善重要医疗防护物资的产能储备和技术储备提供了有力支撑。
- 规范市场秩序:通过严格的注册审批,确保上市产品安全有效,维护了公平竞争的市场环境,保护了使用者权益。
四、 后续监管要求
北京市药品监督管理局要求:
- 注册人(生产企业) 须严格落实产品质量安全主体责任,确保生产活动持续符合《医疗器械生产质量管理规范》要求,对产品全生命周期质量负责。
- 经营使用单位 应从合法渠道采购已获注册证的医疗器械,并按照产品说明书的要求进行储存、使用和维护。
- 各级药品监督管理部门 将加强对上述产品的上市后监管,组织开展监督检查和监督抽检,严厉打击违法违规行为,确保公众用械安全。
五、 信息查询
相关产品具体注册证号、注册人名称、型号规格等信息,可登录北京市药品监督管理局官方网站“数据查询”栏目进行查询。
特此公告。
北京市药品监督管理局
2025年5月
如若转载,请注明出处:http://www.chinaskinhospital.com/product/83.html
更新时间:2026-04-16 11:42:16